 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
实验测得温度T时反应的速率方程是由此可以得出的结论是()A、该反应一定是基元反应 B、该反应一
A.该反应一定是基元反应
B.该反应一定是复合反应
C.该反应可能是基元反应
D.对A来说是二级反应
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
A.该反应一定是基元反应
B.该反应一定是复合反应
C.该反应可能是基元反应
D.对A来说是二级反应
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“实验测得温度T时反应的速率方程是由此可以得出的结论是()A、…”相关的问题
更多“实验测得温度T时反应的速率方程是由此可以得出的结论是()A、…”相关的问题
实验测得化学应A+2B-→3C在298.15K时的速率和浓度的关系如下表所示:
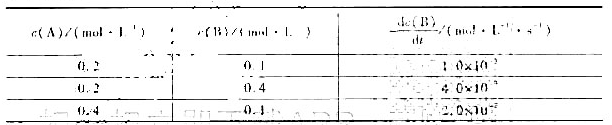 (1)写出反应的速率方程;
(1)写出反应的速率方程;
(2)求出反应级数:
(3)求反应的速率常数。
实验测得反应
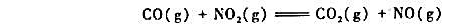
650K时的数据如下:
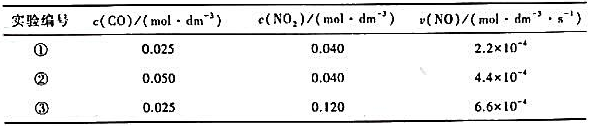
(1)通过推理写出反应的速率方程;
(2)求650K时的速率常数;
(3)当c(CO)=0.10mol·dm-3,c(NO2)=0.16mol·dm-3时,求650K时的反应速率;
(4)若800K时的速率常数为23.0dm3·mol-1·s-1,求反应的活化能。
某反应A→C+D的速率方程为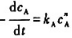 在300K下开始反应时只有A.实验过程中测得以下数据:
在300K下开始反应时只有A.实验过程中测得以下数据:

则此反应的级数为().
A.零级
B.一级
C.3/2级
D.二级
实验表明,在一定温度范围内,反应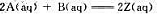 符合质量作用定律。该反应的速率方程为();该反应的级数为();若其他条件()不变,将A的浓度增加到原来的3倍,则反应速率增大到原来速率的()。
符合质量作用定律。该反应的速率方程为();该反应的级数为();若其他条件()不变,将A的浓度增加到原来的3倍,则反应速率增大到原来速率的()。
NOCI分解反应为2NOCI→2NO+Cl2实验测得NOCI的浓度与时间的关系如下:
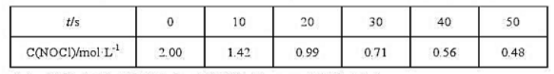
求各时间段内反应的平均速率:用作图法求t=25s时的瞬时速率。
660K时的反应2NO+02→2NO2NO和O2的初始浓度c(NO)和c(O2)及反应初始速率v的实验数据为:
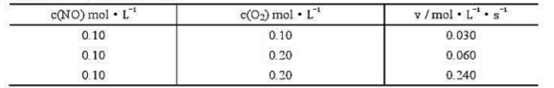
(1)写出反应的速率方程
(2)求反应的级数和速率常数
(3)求c(NO)=c(O2)=0.15molL-1时的反应速率。
在一定条件下,反应H2(g)+Br2((g)→2HBr(g)的速率方程符合速率方程的一般形式,即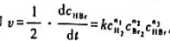 .
.
在某温度下,当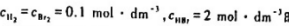 时,反应速率为v.其他不同浓度时的速率如下表所示:
时,反应速率为v.其他不同浓度时的速率如下表所示:

求反应的分级数n1、n2、n3.
浓度和初始速率,见表3-2.

(1)写出反应速率方程
(2)计算25℃下反应速率系数;
(3)计算当c(C5H5N)=5.0x10-5mol·L-5,c(CH3l)=2.0x10-5mol·L-1时,相应的初始速率.
某温度下乙醛的分解反应为
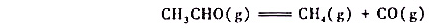
根据下列实验数据:

(1)分别求算42-242s和242-665s时间间隔的平均反应速率,并说明二者大小不等的原因;
(2)利用作图法求出t=100s时的瞬时反应速率。