 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
[主观题]
解释下列现象:(1)用KMnO4滴定C2O42-时,滴定KMnO4的红色消失速度由慢到快:(2
解释下列现象:(1)用KMnO4滴定C2O42-时,滴定KMnO4的红色消失速度由慢到快:(2
)间接碘量法测定铜时,若试液中有Fe3+;AsO43-,它们都可将碘离子氧化成碘单质,加入NH4HF2可消除两者的干扰,解释其中原因。
查看答案
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
)间接碘量法测定铜时,若试液中有Fe3+;AsO43-,它们都可将碘离子氧化成碘单质,加入NH4HF2可消除两者的干扰,解释其中原因。
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“解释下列现象:(1)用KMnO4滴定C2O42-时,滴定KM…”相关的问题
更多“解释下列现象:(1)用KMnO4滴定C2O42-时,滴定KM…”相关的问题
A.#图片0$#
B.#图片1$#
C.#图片2$#
D.#图片3$#
用KMnO4标准溶液滴定Fe2+的反应为:

试计算:①该反应的平衡常数;②为使反应完全定量进行(Fe2+≤10-3[Fe3+]),所需的最低[H+]是多少?(已知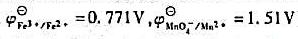 )
)
B.NaNO2液滴定磺胺嘧啶
C.Na2S2O3液滴定I2液
D.Karl Fischer法测定微量水
E.Fe2+液滴定KMnO4液