 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
用已知浓度的NaOH标准溶液,滴定相同浓度不同弱酸时,如果弱酸Ka值越大,则:()。
A.终点时,指示剂颜色变化越不明显
B.消耗NaOH的量越多
C.消耗NaOH的量越小
D.滴定突跃范围越大
E.滴定突跃范围越小
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
A.终点时,指示剂颜色变化越不明显
B.消耗NaOH的量越多
C.消耗NaOH的量越小
D.滴定突跃范围越大
E.滴定突跃范围越小
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“用已知浓度的NaOH标准溶液,滴定相同浓度不同弱酸时,如果弱…”相关的问题
更多“用已知浓度的NaOH标准溶液,滴定相同浓度不同弱酸时,如果弱…”相关的问题
酸的离解常数Ka。
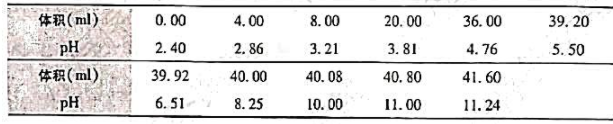
A.甲基红作指示剂,滴定误差小
B.阶酞作指示剂,滴定误差小
C.两种方法滴定误差没有差别
D.无法判断
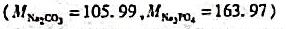
A.H2SO4溶液和HAc溶液中的氢离子浓度相等
B.H2SO4溶液的氢离子浓度是HAc溶液的氢离子浓度的2倍
C.H2SO4溶液的浓度与HAc溶液的浓度相等
D.H2SO4溶液的浓度是HAc溶液的浓度的1/2
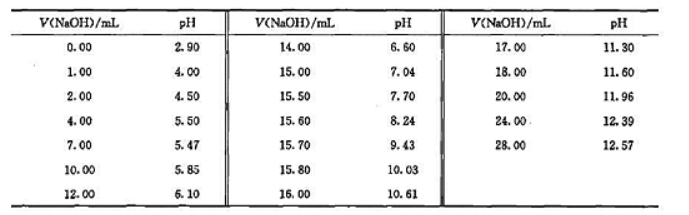
(1)绘制pH-V(NaOH)的曲线,从曲线的拐点确定测定终点.
(2)绘制ΔpH-V(NaOH)的曲线,从曲线的最高点确定测定终点.
(3)用二次微商计算法,从曲线的最高点确定滴定终点.
(4)根据(3)的值计算HCI的浓度.
A.误差的积累会对结果有较大影响
B.滴定引起的误差大于称量引起的误差
C.用基准试剂直接标定时其组成不变
D.用已知准确浓度的标准溶液标定时,其组成可能会变
含H2SO4(Mr=98.07)和H3PO4(Mr=98.00)的混合液两份(体积均为25.00mL),分别用0.1018mol·L-1的NaOH标准溶液滴定。第一份以甲基橙(pKHn=3.4)作指示剂,需25.18mL 滴至终点;第二份以酚酞(pKHn=9.1)作指示剂,需35.22mL到达终点。试求混合液中每种酸的浓度?(已知H3PO4的Ka1=10-2.12,Ka2=10-7.21,Ka3=10-12.7)
A.化学计量点前0.1%的pH值减小,化学计量点后0.1%的pH值不变
B.化学计量点前0.1%的平pH值减小,化学计量点后0.1%的pH值增大
C.化学计量点前后0.1%的pH值均减小
D.化学计量点前后0.1%的pH值均增大
E.化学计量点前0.1%的pH值不变,化学计量点后0.1%的pH值增大
A.以上指示剂均不可
B.酚酞
C.中性红(变色范围pH6.8~8.0)
D.铬黑T
E.A和B均可