 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
主族元素R最高价氧化物对应水化物的化学式为H2RO3,则其氢化物的化学式是()
A.HR
B.RH4
C.H2R
D.RH3
 答案
答案
B、RH4
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
A.HR
B.RH4
C.H2R
D.RH3
 答案
答案
B、RH4
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“主族元素R最高价氧化物对应水化物的化学式为H2RO3,则其氢…”相关的问题
更多“主族元素R最高价氧化物对应水化物的化学式为H2RO3,则其氢…”相关的问题
下表是元素周期表中的一部分,回答下列问题: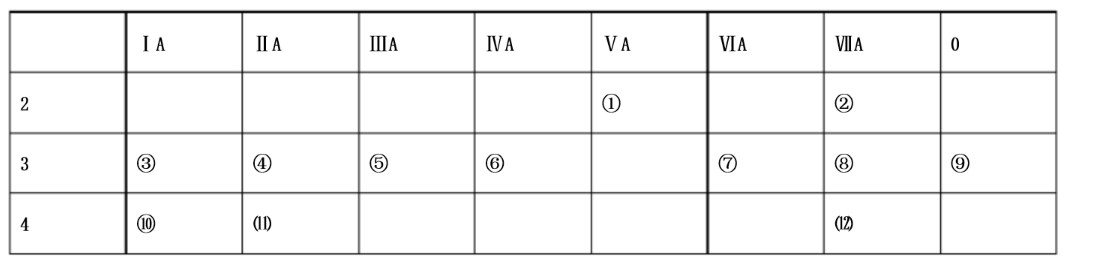 (1)写出下列元素名称①(),⑤(),⑨(),⑾()。
(1)写出下列元素名称①(),⑤(),⑨(),⑾()。
(2)在这些元素中,金属性最强的元素是()﹔除稀有气体元素以外的元素中原子半径最大的是(),原子半径最小的是()。其氢化物最稳定的是()。(填写元素符号)
(3)元素②和③形成的离子的电子层结构()(填“相同”或“不相同”),两者形成的化合物是否是离子化合物()(填“是”或“否”),该化合物的电子式为()。
(4)元素⑧的最高价氧化物对应的水化物化学式为:()名称为()。
(5)在这些元素的最高价氧化物对应的水化物中,属于两性氢氧化物的是()(填写化学式),写出其和盐酸反应的化学方程式()。
A.元素A、B组成的化合物常温下一定呈气态
B.一定条件下,元素C、D的最高价氧化物对应的水化物都是强碱
C.工业上常用电解法制备元素C、D、E的单质
D.化合物AE与CE有相同类型的化学键
(1)A的元素符号为(),其在元素周期表的位置:第()周期,第()族。
(2)元素A、B形成的最简单的气态氢化物稳定性较强的是()(填化学式),元素C和D可形成化合物DC2,其电子式为()。
(3)F的单质加入到D的最高价氧化物对应水化物的溶液中,发生反应的离子方程式为();上述反应的气体产物和C元素的单质设计成的燃料电池已用于航天飞机。试写出以30%KOH溶液为电解质溶液的这种电池在工作时负极的电极反应式为()。
(4)工业制取E的化学反应方程式为()。
A.丁的最高价氧化物是人类将太阳能转换为电能的常用材料
B.气态氢化物的稳定性:庚<己<戊
C.常温下,甲和乙的单质均能与水剧烈反应
D.丙与戊的原子序数相差28
A.Z的氢化物的酸性比WX2的水化物的强,说明Z的非金属性比W的强
B.离子半径大小:Z>Y>X
C.工业上用MnO2和Z的氢化物的浓溶液在加热的条件下制取Z的单质
D.能形成WXZ2这种共价化合物
A.X2W、X2Y的水溶液都呈碱性
B.原子半径:r(Z)>r(Y)>r(X)>r(W)
C.简单气态氢化物的热稳定性:W
D.W与氢元素形成的化合物分子中一定不含非极性共价键
A.氯乙烷属于氧化物
B.氯乙烷由碳、氢、氯原子构成
C.氯乙烷中氯元素的质量分数最大
D.氯乙烷中碳、氢、氯元素的质量比为2︰5︰1