 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
已知BaSO4的溶度积Ksp=1.1×10-16,将0.1mol/L的BaCl2溶液和0.01mol/L的H2SO4溶液等体积混合,则溶液()。
A.无沉淀析出
B.有沉淀析出
C.析出沉淀后又溶解
D.不一定
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
A.无沉淀析出
B.有沉淀析出
C.析出沉淀后又溶解
D.不一定
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“已知BaSO4的溶度积Ksp=1.1×10-16,将0.1m…”相关的问题
更多“已知BaSO4的溶度积Ksp=1.1×10-16,将0.1m…”相关的问题
A.BaSO4(Ksp=1.1×10-10)
B.Mg(OH)2(Ksp=1.8×10-11)
C.PbI2(Ksp=7.1×10-9)
D.AgIO3(Ksp=3.0×10-8)
已知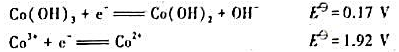
若用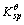 (1)表示Co(OH)3的溶度积常数,
(1)表示Co(OH)3的溶度积常数,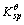 (2)表示Co(OH)2的溶度积常数,试求
(2)表示Co(OH)2的溶度积常数,试求 (1)/
(1)/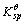 (2)的值。
(2)的值。
已知25°C时AgBr的溶度积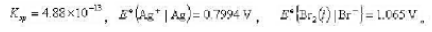 试计算25°C时
试计算25°C时
(1)银-溴化银电极的标准电极电势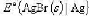 ;
;
(2)AgBr(s)的标准生成吉布斯函数。
根据Mg(OH)2的溶度积计算:
(1)Mg(OH)2在水中的溶解度(mol·L-1);
(2)Mg(OH)2饱和溶液中的c(Mg2+),c(OH-)和pH;
(3)Mg(OH)2在0.010nool.L-1NaOH溶液中的溶解度(mol·L-1);
(4)Mg(OH)2在0.010mol·L-1MgCl2溶液中的溶解度(mol·L-1).
298.15K时,Mg(OH)2的标准溶度积常数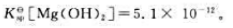 试计算:
试计算:
(1)Mg(OH)2在水中的溶解度:
(2)Mg(OH)2饱和溶液中的Mg2+、OH-的浓度和溶液的pH;
(3)Mg(OH)2在0.010mol·L-1NaOH溶液中的溶解度;
(4)Mg(OH)2在0.010mol·L-1MgCl2溶液中的溶解度。
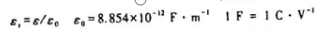
反应A+2B→D的速率方程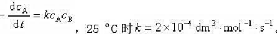
(1)若初始溶度cA,O=0.02md·dm-3,cB,O=0.04mol·dm-3,求t1。
(2)若将反应物A与B的挥发性固体装入5dm3密闭容器中,已知25°C时A和B的饱和蒸气压分别为10kPa和2kPa,问25°C时0.5molA转化为产物需多长时间?
A.离子积>溶度积,过饱和溶液,析出沉淀
B.离子积=溶度积,饱和溶液,动态平衡
C.离子积<溶度积,不饱和溶液,无沉淀析出
D.离子积<溶度积,若有沉淀,则不溶解