 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
在密闭容器中进行反应:X2(g)+Y2(g) ⇌2Z(g),已知X2、Y2、Z的起始浓度分别为0.1 mol•L-1、0.3 mol•L-1、0.2 mol•L-1,在一定条件下,当反应达到平衡时,各物质的浓度有可能是()
A.Z为0.3 mol•L-1
B.Y2为0.4 mol•L-1
C.X2为0.2 mol•L-1
D.Z为0.4 mol•L-1
 答案
答案
A、Z为0.3 mol•L-1
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
A.Z为0.3 mol•L-1
B.Y2为0.4 mol•L-1
C.X2为0.2 mol•L-1
D.Z为0.4 mol•L-1
 答案
答案
A、Z为0.3 mol•L-1
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“在密闭容器中进行反应:X2(g)+Y2(g) ⇌2Z(g),…”相关的问题
更多“在密闭容器中进行反应:X2(g)+Y2(g) ⇌2Z(g),…”相关的问题
已知A(g)的分解反应为一级反应。在560K的真空密闭恒容容器中充入初始压力为21.33kPa的氮甲烷气体,反应进行1000s时测得系统的总压为22.73kPa,求速率常数kp,A及半衰期t1/2。
偶氮甲烷(CH3NNCH3)气体的分解反应
(CH3NNCH3)(g)→C2H6(g)+N2(g).
为一级反应.在287℃的真空密闭恒容容器中充入初始压力为21.332kPa的偶氮甲烷气体,反应进行1000s时测得系统的总压为22.732kPa,求速率常数k及半衰期t1/2.
A.当v(CO)(正)=v(H2)(正),时,反应达到平衡状态
B.其他条件不变,适当增加C(s)的质量会使平衡正向移动
C.保持容器体积不变,充入少量He使体系压强增大,反应速率一定增大
D.其他条件不变,仅将容器的体积缩小一半,再次达到平衡时,H20(g)的平衡浓度可能是原来的2.1倍
密闭容器中的反应CO(g)+H2O(g)=CO2(g)+H2(g)在750K时其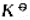 =2.6,试计算:
=2.6,试计算:
(1)当原料气中H2O(g)和CO(g)的物质的量之比为1:1时,CO(g)的转化率为多少?
(2)当原料气中H2O(g)和CO(g)的物质的量之比为4:1时,CO(g)的转化率为多少 ? 说明什么问题?
A.平衡后升高温度,容器中气体颜色加深
B.每消耗44.8LNO2,生成N2O4的分子数一定为NA
C.该容器中气体质量为46g时,原子总数为3NA
D.若N2O4分子数增加0.5NA,则放出0.5akJ的热量
A.气体总质量不变
B.混合气体密度不变
C.反应物B的浓度不变
D.混合气体平均相对分子质量不再改变
A.3,2
B.3,1
C.1,0
D.2,1
在一定温度下,将1.0molNa2O2(g)放入一密闭容器中,发生下列可逆反应
 当达到化学平衡时,容器内有0.8molNO,气体总压为100kPa。则该可逆反应在此温度下的标准平衡常数为().
当达到化学平衡时,容器内有0.8molNO,气体总压为100kPa。则该可逆反应在此温度下的标准平衡常数为().
A、0.40
B、0.67
C、0.76
D、1.3
A.NaHCO3和NaOH
B.Na2CO3和NaOH
C.NaHCO3和Na2CO3
D.只有Na2CO3