 更多“氢燃料电池是利用哪两种物质反应产生能源的?()”相关的问题
更多“氢燃料电池是利用哪两种物质反应产生能源的?()”相关的问题
第5题
过度排放CO2会造成”温室效应“,科学家正在研究如何将CO2转化为可以利用的资源,其中一种方案就是将CO2转化为可再生燃料甲醇(CH3OH)。其化学方程式为: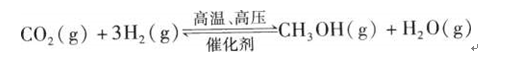
请填空:
问题一、写出上述反应的平衡常数表达式K=()。
问题二、在容积为2L的密闭容器中,用一定量二氧化碳与一定量氢气在一定条件下合成甲醇,实验结果如下图。以下说法正确的选项是()。
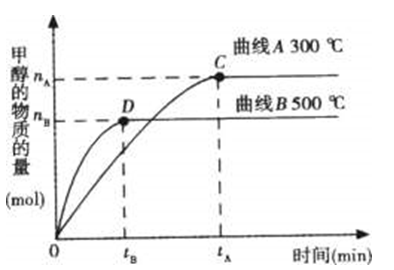
A在300℃,从反应开始到平衡,甲醇的平均反应速率
B反应体系从300℃升温到500℃,平衡常数K变大
C该反应的正反应为放热反应
D处于C点的反应体系从300℃升温到500℃n(H2)/n(CH3OH)增大
问题三、25℃、1.01×105Pa时16g液态甲醇完全燃烧,当恢复至原状态时,放出362.9kJ热量,此反应的热化学方程式为()。
问题四、选用合适的合金为电极,以氢氧化钠、甲醇、水、氧气为原料,可以制成一种以甲醇为原料的燃料电池,此燃料电池负极应加入或通入的物质是,正极的电极反应式为()。
第6题
截至2020年底,全球氢燃料电池汽车保有量较上一年度增长38%。氢能的大规模应用正从汽车领域逐步拓展至其他交通、建筑和工业等领域。应用在轨道交通和船舶上,氢能可降低长距离、高负荷交通运输对传统油气燃料的依赖。应用于分布式发电,氢能可为家庭住宅、商业建筑供电供暖。氢能还可直接为石化、钢铁、冶金等行业提供高效原料、还原剂和高品质热源,有效减少碳排放。这段文字着重介绍的是()
A.氢能热效率高于传统能源
B.氢能利用将取代传统的工业原料
C.氢能有着多元的应用场景
D.氢能利用将成为节能减排新举措
第7题
下列对文本内容的理解和分析,正确的一项是()
A.氢的单质形态是氢气,它是一种无色无味无臭,极易燃烧的由双原子分子组成的气体
B.氢燃料电池所需的氢气是利用风能,太阳能通过电解水方式以及从工业废气中提纯两种渠道获取的
C.改革开放时,中国已成为世界汽车制造大国,不论是市场还是技术都处于世界领先地位
D.中国政府对氢燃料电池汽车产业给予了高度的重视,相信未来必将有更快的发展


 如果结果不匹配,请
如果结果不匹配,请 

















