 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
在燃烧热实验中,需用作图法求取反应前后真实的温度改变值ΔT,主要是因为()。
A.温度变化太快,无法准确读取
B.校正体系和环境热交换的影响
C.消除由于略去有酸形成放出的热而引入的误差
D.氧弹计绝热,必须校正所测温度
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
A.温度变化太快,无法准确读取
B.校正体系和环境热交换的影响
C.消除由于略去有酸形成放出的热而引入的误差
D.氧弹计绝热,必须校正所测温度
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“在燃烧热实验中,需用作图法求取反应前后真实的温度改变值ΔT,…”相关的问题
更多“在燃烧热实验中,需用作图法求取反应前后真实的温度改变值ΔT,…”相关的问题
NOCI分解反应为2NOCI→2NO+Cl2实验测得NOCI的浓度与时间的关系如下:
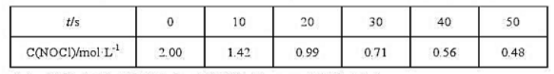
求各时间段内反应的平均速率:用作图法求t=25s时的瞬时速率。
某温度下乙醛的分解反应为
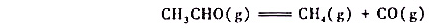
根据下列实验数据:

(1)分别求算42-242s和242-665s时间间隔的平均反应速率,并说明二者大小不等的原因;
(2)利用作图法求出t=100s时的瞬时反应速率。
此题为判断题(对,错)。
钛(Ti)被称为继铁、铝之后的第三金属,四川攀枝花和西昌地区的钒钛磁铁矿储量十分丰富。如以下图所示,将钛厂、氯碱厂和甲醇厂组成产业链可以大大提高资源利用率,减少环境污染。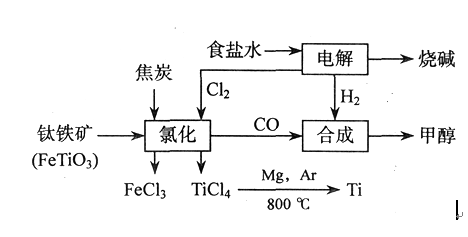 请填写以下空白:
请填写以下空白:
问题一、电解食盐水时,总反应的离子方程式是()。
问题二、写出钛铁矿经氯化法得到四氯化钛的化学方程式:()。
问题三、已知:①Mg(s)+Cl2(g)=MgCl2(s);△H=-641kJ/mol ②Ti(s)+2Cl2(g)=TiCl4(s);△H=-770kJ/mol。以下说法正确的选项是()。
AMg的燃烧热为641kJ/mol
BTi的能量一定比TiCl4高
C等质量的Mg(s)、Ti(s)与足量的氯气反应,前者放出的热量多
D该冶炼Ti法对环境友好
问题四、在上述产业链中,合成192t甲醇理论上需额外补充H2()t(不考虑生产过程中物质的任何损失)。
问题五、以甲醇、空气、氢氧化钾溶液为原料,石墨为电极可构成燃料电池。该电池中负极上的电极反应式是()。
A.红磷燃烧前后质量的测定:红色固体燃烧,发光放热,产生黄白色火焰,天平平衡
B.铁钉与硫酸铜溶液反应前后质量的测定:银白色固体表面有紫红色固体析出
C.铜丝表面的氧化铜与氢气在加热条件下反应:试管口有水雾产生
D.向蒸馏水中滴入石蕊溶液,再向试管中通入二氧化碳:无色溶液先变为红色,然后红色溶液变为紫色
A.△H是CO2(g)的生成热
B.△H是CO(g)的燃烧热
C.△H<0
D.△H=△U