 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
对于反应2H2(g)+O2(g)===2H2O(g)【放热反应】的能量变化描述正确的是()
A.成键过程中吸收能量
B.断键过程中吸收能量,成键过程中释放能量
C.断键过程中释放能量
D.断键过程中释放能量,成键过程中吸收能量
 答案
答案
B、断键过程中吸收能量,成键过程中释放能量
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
A.成键过程中吸收能量
B.断键过程中吸收能量,成键过程中释放能量
C.断键过程中释放能量
D.断键过程中释放能量,成键过程中吸收能量
 答案
答案
B、断键过程中吸收能量,成键过程中释放能量
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“对于反应2H2(g)+O2(g)===2H2O(g)【放热反…”相关的问题
更多“对于反应2H2(g)+O2(g)===2H2O(g)【放热反…”相关的问题
利用标准摩尔生成炕数据计算下列反应的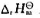 及
及 假定反应中的各气体都可视作理想气体。
假定反应中的各气体都可视作理想气体。
(1)H2S(g)+O2(g)=H2O(1)+SO2(g)
(2)CO(g)+2H2(g)=CH3OH(1)
烟气的脱硫(除SO2)技术和脱硝(除NOx)技术都是环境科学研究的热点。
问题一、选择性催化复原法的脱硝原理为:

①上述反应中每转移3mol电子,生成标准状况下N2的体积为()L。
②已知:2H2(g)+O2(g)=2H2O(g)ΔH=-483.6kJ•mol-1
N2(g)+3H2(g)=2NH3(g)ΔH=-92.4kJ•mol-1
N2(g)+O2(g)=2NO(g)ΔH=-180.5kJ•mol-1
则反应6NO(g)+4NH3(g)=5N2(g)+6H2O(g)的ΔH=()。
问题二、目前,科学家正在研究一种以乙烯作为复原剂的脱硝(NO)原理,其脱硝机理示意图如以下图1,脱硝率与温度、负载率(分子筛中催化剂的质量分数)的关系如图2所示。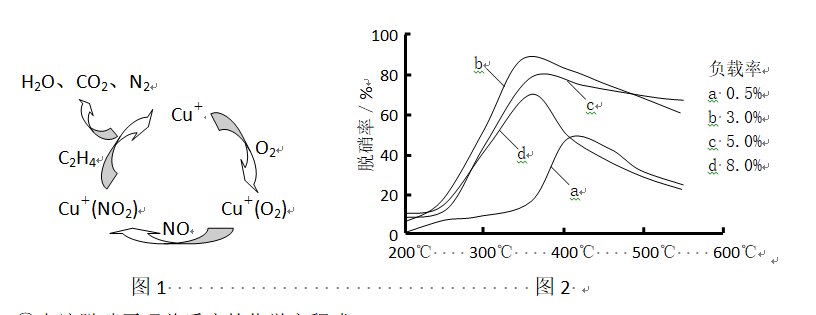
①出该脱硝原理总反应的化学方程式:()。
②为到达最正确脱硝效果,应采取的条件是()。
A.1∶1
B.1∶2
C.2∶3
D.3∶2
上又应用什么方法更好?为什么?
(1)SnO2(s)→Sn(s)+O2(g)
(2)SnO2(s)+C(s)—Sn(s)+CO2(g)
(3)SnO2(s)+2H2(g)→Sn(s)+2H2O(g)
A.2 500
B.100
C.4×10-4
D.2×10-2
已知反应SnO2(s)+2H2(g)=Sn(s)+2H2O(g)和CO(g)+H2O(g)=CO2(g)+H2(g)的平衡常数分别为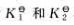 。则反应SnO2(s)+2CO(g)=2CO2(g)+Sn(s)
。则反应SnO2(s)+2CO(g)=2CO2(g)+Sn(s)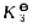 的=()。
的=()。
问题1、1840年Devil用干燥的氧气通过干燥的硝酸银,得到N2O5,该反应的氧化产物是一种参与大气循环的气体,写出该反应的化学方程式()。
问题2、F.Daniels等曾利用测压法在刚性反应器中研究了25℃时N2O5(g)分解反应
2N205(g)→4NO2(g)+O2(g)+Q1(Q1<0),2NO2(g) N204(g)+Q2(Q2>0)
N204(g)+Q2(Q2>0)
其中NO2二聚为N2O4的反应可以迅速达到平衡。体系的总压强P随时间t的变化如下表所示(t=00时,N2O5(g)完全分解);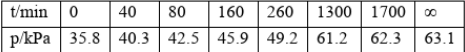
①究表明,N2O5(g)分解的速率v=2x10-3Xpn2o5(kPa'min)。t=62min时,测得体系Po2=2.9kPa,则此时PN2O5:=()kPa,v=()(kPa/min)。
②若提高反应温度至35℃,则N2O5(g)完全分解后体系压强P00(35℃)()63.1kPa(填“大于”、“等于”或“小于”),试从勒夏特列原理的角度加以解释()。
③写岀N2O4(g) 2NO2(g)反应的平衡常数表达式()。
2NO2(g)反应的平衡常数表达式()。
问题3、对于反应2N2O5(g)→4NO2(g)+O2(g),R.A.Ogg提出如下反应历程:
第一步:N2O5 NO2+NO3快速平衡
NO2+NO3快速平衡
第二步NO2+NO3→NO+NO2+O2慢反应
第三步NO+NO3→2NO2快反应
其中可近似认为第二步反应不影响第一步的平渐。下列表述错误的是()(填编号),
A.v(第一步反应的逆反应)>v(第二步反应)B.反应的中间产物只有NO3
C、该反应的速率主要由第二步决定D.N2O5的分解率主要由第一步决定
A.#图片1$#
B.#图片2$#
C.#图片3$#
D.#图片4$#