 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
已知AgCl的=1.8×10-10,试求AgCl饱和溶液的c(Ag+);若加入中盐酸,使溶液的pH=3.0,
已知AgCl的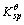 =1.8×10-10,试求AgCl饱和溶液的c(Ag+);若加入中盐酸,使溶液的pH=3.0,再求溶液的c(Ag+)。
=1.8×10-10,试求AgCl饱和溶液的c(Ag+);若加入中盐酸,使溶液的pH=3.0,再求溶液的c(Ag+)。
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
已知AgCl的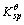 =1.8×10-10,试求AgCl饱和溶液的c(Ag+);若加入中盐酸,使溶液的pH=3.0,再求溶液的c(Ag+)。
=1.8×10-10,试求AgCl饱和溶液的c(Ag+);若加入中盐酸,使溶液的pH=3.0,再求溶液的c(Ag+)。
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“已知AgCl的=1.8×10-10,试求AgCl饱和溶液的c…”相关的问题
更多“已知AgCl的=1.8×10-10,试求AgCl饱和溶液的c…”相关的问题
A.AgCl和Ag2CrO4的溶解度可由两者溶度积求得
B.AgCl和Ag2CrO4两者类型不同,不能用溶度积直接比较溶解度大小
C.AgCl溶解度大于Ag2CrO4
D.AgCl和Ag2CrO4都是难溶盐
E.AgCl和Ag2CrO4两者的IP大于各自溶度积时开始沉淀
F.向有[Cl-]、[CrO42-]存在的溶液中逐滴加硝酸银溶液,AgCl先出现
NH4Cl和NH3·H2O的混合溶液,其pH=9.5,已知NH3·H2O的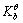 =
=
1.8×10-5。若溶液中c(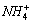 )为5.0mol·dm-3,试求溶液的c(NH3·H2O)。
)为5.0mol·dm-3,试求溶液的c(NH3·H2O)。
试求算0.20mol·dm-3氨水中OH-的浓度,H+的浓度和溶液的pH。向其中加人固体NH4Cl,使NH4+的浓度达到1.0×10-2mol·dm-3,再求体系中OH-的浓度和pH。已知氨水的Kb=1.8×10-5.
求在100cm3浓度为10mol·dm-3的氨水中能溶解多少克AgC1固体?已知[Ag(NH3)2]+的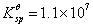 ,AgCl的
,AgCl的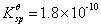 。
。
A.氨水(Kb=1.8×10-5)
B.苯酚(Kb=1.1×10-10)
C.NH4+
D.H3BO3(Ka=5.8×10-10)
A.0.1mol/LHF(Ka=6.8×10-4)
B.0.1mol/LHCN(Ka=4.9×10-10)
C.0.1mol/LNH4Cl(Kb=1.8×10-5)
D.0.1mol/LNaAc(Ka=1.8×10-5)
A.BaSO4(Ksp=1.1×10-10)
B.Mg(OH)2(Ksp=1.8×10-11)
C.PbI2(Ksp=7.1×10-9)
D.AgIO3(Ksp=3.0×10-8)