题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
[单选题]
现代价键理论认为,两个原子相互接近时,只有自旋()的两个单电子可以相互配对,使核间电子云密度(),使体系能量(),形成()的共价键。
A.相反;降低;增大;稳定
B.相同;减低;增大;稳定
C.相同;增大;降低;稳定
D.相反;增大;降低;稳定
查看答案
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
A.相反;降低;增大;稳定
B.相同;减低;增大;稳定
C.相同;增大;降低;稳定
D.相反;增大;降低;稳定
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“现代价键理论认为,两个原子相互接近时,只有自旋()的两个单电…”相关的问题
更多“现代价键理论认为,两个原子相互接近时,只有自旋()的两个单电…”相关的问题
A.N2分子包含一个s键和两个π键
B.CO分子中存在配位键
C.原子形成共价键时必须遵守饱和性和方向性原则
D.sp2杂化轨道是由1s和2p轨道杂化而成
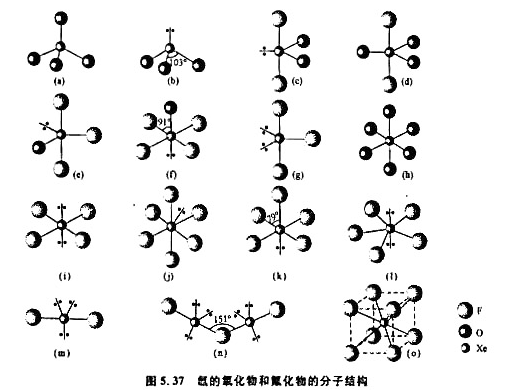
图5.37示出氙的氟化物和氧化物的分子(或离子)结构。
(1)根据图形及VSEPR理论,指出分子的几何构型名称和所属点群;
(2)Xe原子所用的杂化轨道;
(3)Xe原子的表观氧化态;
(4)已知在XeF2,XeF4,加合物晶体中,两种分子的构型与单独存在时的几何构型相同,不会相互化合成XeF2,从中说明什么问题?