 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
[单选题]
反应系统温度最低的地方是在()。
A.反应器扩大段以下0.3~0.6m
B.循环气压缩机入口
C.循环气压缩机出口
D.循环气冷却器出口
查看答案
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
A.反应器扩大段以下0.3~0.6m
B.循环气压缩机入口
C.循环气压缩机出口
D.循环气冷却器出口
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“反应系统温度最低的地方是在()。”相关的问题
更多“反应系统温度最低的地方是在()。”相关的问题
夏季在空调房里,温度最低的位置是:()。
A 靠近屋顶的地方
B 靠近地板的地方
C 屋顶和地板中间的地方
D 靠近窗口的地方
A.回到岗位不作任何处理,但要防止再次超压
B.按程序停车
C.对法兰消漏处用氮气或者蒸汽进行吹扫、稀释
D.降低反应温度、压力使反应负荷最低
在一定的温度下Ag2O(s)和AgNO3(s)受热均能分解.反应为
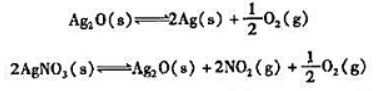
假定反应的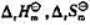 不随温度的变化而改变,估算Ag2O(s)和AgNO3(s)按上述反应方程式进行分解时的最低温度,并确定AgNO3,分解的最终产物.
不随温度的变化而改变,估算Ag2O(s)和AgNO3(s)按上述反应方程式进行分解时的最低温度,并确定AgNO3,分解的最终产物.
反应
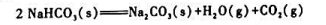
在不同温度时的平衡总压如下:
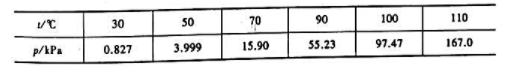
设反应的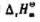 与温度无关.求:
与温度无关.求:
(1)上述反应的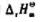 ;
;
(2)lg(p/kPa)与T的函敷关系式;
(3)NaHCO3的分解温度.
用KMnO4标准溶液滴定Fe2+的反应为:

试计算:①该反应的平衡常数;②为使反应完全定量进行(Fe2+≤10-3[Fe3+]),所需的最低[H+]是多少?(已知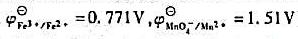 )
)
A.高温下,脱烷基和裂解反应容易进行
B.温度升高,催化剂积炭速度加快,催化剂的活性下降速度加快
C.由于异构化反应是微放热反应,因此升高温度后,对二甲苯的平衡浓度变化不大
D.二甲苯异构化反应是吸热反应,降低反应温度,对反应有利
反应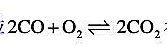 在2800K、101325Pa下达到平衡,平衡常数
在2800K、101325Pa下达到平衡,平衡常数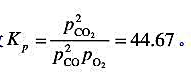 求:
求:
(1)这时的离解度及各气体的分压力;
(2)在相同温度下,下列两反应各自的平衡常数.
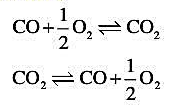
A.升高温度可使化学平衡向正反应方向移动
B.#图片1$#
C.反应物的分压等于生成物的分压
D.加入催化剂,可使化学平衡向正反应方向移动