题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
[主观题]
已知乙醇(C2H5OH)在351K和100kPa大气压下正常沸点温度(351K)时的蒸发热为39.2kJ·mol,
已知乙醇(C2H5OH)在351K和100kPa大气压下正常沸点温度(351K)时的蒸发热为39.2kJ·mol,
试估算1molC2H5OH(l) 在该蒸发过程中的△U。
查看答案
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
试估算1molC2H5OH(l) 在该蒸发过程中的△U。
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“已知乙醇(C2H5OH)在351K和100kPa大气压下正常…”相关的问题
更多“已知乙醇(C2H5OH)在351K和100kPa大气压下正常…”相关的问题
r=1.11x10-9Pa-1,摩尔定压热容Cp,m=114.30J·mol-1·K-1,密度ρ=0.7893g·cm-3.求20℃时液态乙醇的CV,m.
气相总压p=24.832kPa,试计算水的活度及活度因子.假设水的摩尔蒸发炜在50~100℃可按常数处理.已知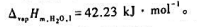
冰(H2O,s)在100kPa下的熔点为0℃,此条件下的摩尔融化焓 =6.012kJ·mol-1.已知在-10~0℃范围内过冷水(H2O,l)和冰的摩尔定压热容分别为76.28J·mol-1·K-1和37.20J·mol-1·
=6.012kJ·mol-1.已知在-10~0℃范围内过冷水(H2O,l)和冰的摩尔定压热容分别为76.28J·mol-1·K-1和37.20J·mol-1·
K-1.求在常压及-10℃下过冷水结冰的摩尔凝固焓.
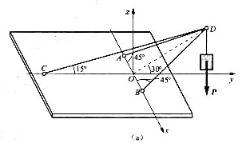
链A,B,C的约束力。