 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
碳60的结构是由()的特殊的分子构型以及量子尺寸效应,才使得碳如此稳定,因而表现出了异常高的化学活性、催化活性。
A.正五边形
B.正五边形和正六边形
C.以上都不对
D.正六边形
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
A.正五边形
B.正五边形和正六边形
C.以上都不对
D.正六边形
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“碳60的结构是由()的特殊的分子构型以及量子尺寸效应,才使得…”相关的问题
更多“碳60的结构是由()的特殊的分子构型以及量子尺寸效应,才使得…”相关的问题
A.迁移率与DNA分子的构型和大小相关,而与DNA分子中的碱基组成和顺序无关
B.迁移率与DNA分子的构型和大小以及DNA分子中的碱基组成和顺序都相关
C.迁移率与DNA分子的构型和大小无关,而与DNA分子中的碱基组成和顺序相关
D.迁移率与DNA分子的构型和大小以及DNA分子中的碱基组成和顺序都无关
(1)当多面体只由五边形面(F5)和六边形面(F6)组成,每个顶点都连接3条棱时,试证明不论由多少个顶点组成多面体,其中五边形面的数目总是12个。
(2)已知C50分子是个具有足球外形的32面体,试计算其价键结构式中的C-C单键数目,C C双键数目和C—C
C双键数目和C—C 键数目。
键数目。
(3)已知C80,C82和C84都能包合金属原子,形成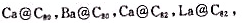
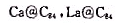 等分子。试分别计算C80,C83和C84分子中含有六边形面的数目。
等分子。试分别计算C80,C83和C84分子中含有六边形面的数目。
(4)气体水合物晶体的结构,可看作由五边形面和六边形面组成的多面体,其中包合气体小分子(如CH4),多面体共面连接而成晶体。试求512,51262,51263等三种多面体(512指含12个五边形面的多面体,51262指含12个五边形面和2个六边形面的多面体)各由几个H2O分子组成,作图表示这些多面体的结构。
A.生铁和钢的性质不同,是由于含碳量不同
B.O和CO2的性质不同,是由于构成它们分子的原子个数不同
C.金刚石和石墨的物理性质不同,由于构成它们的碳原子不同
D.金属钙和铝的性质不同,是由于钙和铝由不同原子构成
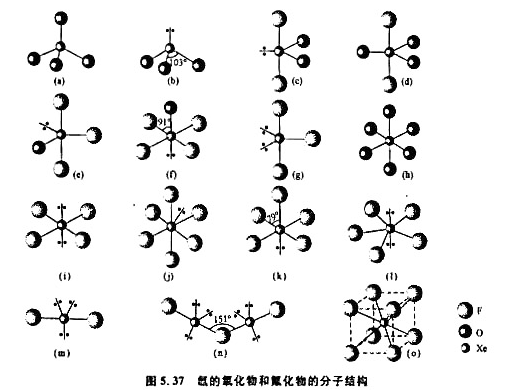
图5.37示出氙的氟化物和氧化物的分子(或离子)结构。
(1)根据图形及VSEPR理论,指出分子的几何构型名称和所属点群;
(2)Xe原子所用的杂化轨道;
(3)Xe原子的表观氧化态;
(4)已知在XeF2,XeF4,加合物晶体中,两种分子的构型与单独存在时的几何构型相同,不会相互化合成XeF2,从中说明什么问题?
A.H2S和NH3均是价电子总数为8的极性分子
B.HS-和HCl均是含一个极性键的18电子粒子
C.H2Cl2和CCl4均是四面体构型的非极性分子
D.SO2和SO3杂化轨道类型均为sp2杂化,立体构型分别为直线形、三角锥形
A.手性碳上的四个原子或基团按次序规则排序
B.由高到低将原子或基团排列连线,若是顺时针,则是R
C.由高到低将原子或基团排列连线,若是顺时针,则是S
D.次序最小的原子或基团放在距观察者较远的位置
A.NF3 是由极性键构成的极性分子
B.氧化产物只有 NF3,还原产物有 NF3 和 NH4F
C.4 mol NH3 被氧化时转移电子的物质的量为 6 mol
D.该条件下 NF3 的氧化性比F2 弱
A.吗啡是由5个环稠合而成的复杂立体结构,左旋吗啡是有效的吗啡构型,而右旋吗啡则无活性
B.吗啡的3位的酚羟基具有弱酸性,17位N-甲基叔胺具有碱性
C.吗啡的第Ⅱ相生物结合主要生成3-葡萄糖苷酸和6-葡萄糖苷酸代谢物
D.在酸性溶液中加热吗啡,可使其脱水并进行分子重排,生成阿扑吗啡,阿扑吗啡可兴奋中枢的呕吐中心,作为催吐剂使用
E.吗啡的17位叔胺易被氧化为N-氧化吗啡,因此吗啡需遮光密闭保存
A、中心原子采取sp3杂化轨道成键的分子,其空间构型一定是四面体
B、CH,分子中的sp3杂化轨道是由H原子的1s轨道和C原子的2p轨道组合而成
C、CH分子中的sp3杂化轨道是由C原了的1s轨道和2p轨道组合而成
D、Sp杂化轨道是由中心原子的最外层s轨道和最外层1个p轨道组合面成