 更多“pH不变时,一元弱酸HA的浓度增大,将导致HA的分布系数增大…”相关的问题
更多“pH不变时,一元弱酸HA的浓度增大,将导致HA的分布系数增大…”相关的问题
第1题
已知相同浓度的一元弱酸的钠盐NaA、NaB、NaC和NaD的水溶液的pH依次增大,则在下列相同浓度的四种一元弱酸溶液中,一元弱酸的解离度最大的是().
A.HA
B.HB
C.HC
D.HD
第3题
由一元弱酸和它的共轭碱NaA组成的缓冲溶液中,HA的浓度为0.25mol·L-1.若在100mL此缓冲溶
由一元弱酸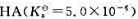 和它的共轭碱NaA组成的缓冲溶液中,HA的浓度为0.25mol·L-1.若在100mL此缓冲溶液中加入5.0mmolNaOH固体,溶液的pH变为5.60。计算加入NaOH固体前缓冲溶液的pH.
和它的共轭碱NaA组成的缓冲溶液中,HA的浓度为0.25mol·L-1.若在100mL此缓冲溶液中加入5.0mmolNaOH固体,溶液的pH变为5.60。计算加入NaOH固体前缓冲溶液的pH.
第4题
25℃时,一元弱酸HA的标准解离常数试计算0.10mol·L-1HA溶液的pH和HA的解离度。
25℃时,一元弱酸HA的标准解离常数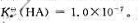 试计算0.10mol·L-1HA溶液的pH和HA的解离度。
试计算0.10mol·L-1HA溶液的pH和HA的解离度。
第6题
某一元弱酸HA试样1.250g用水溶解后稀释至50.00mL.可用41.20mL 0.09000mol·L-1NaOH滴定至计量点,当加入8.24mL NaOH时溶液的pH=4.30.(1)求该弱酸的摩尔质量(2)计算弱酸的解离常数K和计量点的pH(3)选择何种指示剂?
第7题
向0.1摩尔/升的乙酸溶液中,加入相当于0.1摩尔/升的乙酸钠固体(假定加入乙酸钠后体积不变),则溶液氢离子浓度将(),PH值将()。(填入增大、减小或不变)
向0.1摩尔/升的乙酸溶液中,加入相当于0.1摩尔/升的乙酸钠固体(假定加入乙酸钠后体积不变),则溶液氢离子浓度将(),PH值将()。(填入增大、减小或不变)
点击查看答案
第8题
准确量取30.00ml弱酸HA,加水稀释至100ml,在下列电池中为测定电池,以0.1000mol/LNaOH溶液滴定弱
准确量取30.00ml弱酸HA,加水稀释至100ml,在下列电池中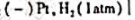
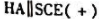 为测定电池,以0.1000mol/LNaOH溶液滴定弱酸HA溶液。当酸被中和一半时,电池电动势为0.524V;化学计量点时,电池电动势为0.749V。(1)计算弱酸HA的Ka;(2)原弱酸HA的浓度是多少?(φSCE=0.242V)。
为测定电池,以0.1000mol/LNaOH溶液滴定弱酸HA溶液。当酸被中和一半时,电池电动势为0.524V;化学计量点时,电池电动势为0.749V。(1)计算弱酸HA的Ka;(2)原弱酸HA的浓度是多少?(φSCE=0.242V)。
第9题
已知集三元弱酸HA则溶液的pH为():0.10mol·L-1NaHA济液的pH为:6.10mol·L-1NaH2
已知集三元弱酸HA则溶液的pH为():0.10mol·L-1NaHA济液的pH为:6.10mol·L-1NaH2
点击查看答案
已知集三元弱酸HA 则
则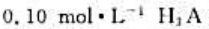
溶液的pH为():0.10mol·L-1NaHA济液的pH为:6.10mol·L-1NaH2A溶液的pH为():9.10mol-1NaH3A溶液的pH为()。
第10题
在一经级除盐系列运行过程中,当阳床未失效时,阴床出水应是()工况。
A.SiO2浓度上升,PH值下降,导电度先微降后又上升,Na+离子浓度上升
B.SiO2浓度,PH值上升,导电度上升,Na+离子浓度稳定不变
C.SiO2浓度上升,PH值下降,导电率先微降后又上升,钠离子浓度稳定不变


 如果结果不匹配,请
如果结果不匹配,请 

















