 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
如图表示某化学反应的微观过程,下列有关说法正确的是()
A.反应前、后原子的种类与数目发生了改变
B.反应物和生成物中都有一种单质
C.甲和丙均为有机物
D.甲的化学式为C2H2
 答案
答案
D、甲的化学式为C2H2
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
A.反应前、后原子的种类与数目发生了改变
B.反应物和生成物中都有一种单质
C.甲和丙均为有机物
D.甲的化学式为C2H2
 答案
答案
D、甲的化学式为C2H2
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“如图表示某化学反应的微观过程,下列有关说法正确的是()”相关的问题
更多“如图表示某化学反应的微观过程,下列有关说法正确的是()”相关的问题
。向(C)的溶液中通入CO2,有白色沉淀(E)析出,(E)不溶于氨水。在较低的温度下加热(E)有(F)生成,(F)易溶于盐酸,也溶于氢氧化钠溶液。但在高温下灼烧(E)后生成的(G)既不溶于盐酸,也不溶于氢氧化钠溶液。试给出(A),(B),(C),(D),(E),(F)和(G)所代表的物质的化学式,并用化学反应方程式表示各过程。
A.研究化学反应的内因与外因对于反应方向与速率的影响;
B.揭示过程的宏观与微观(直至分子水平上)机理;
C.定量地研究总包反应与各个基元反应,基元化学物理反应;
D.研究化学反应能够达到的限度
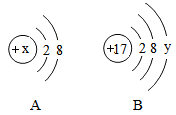
如图中A、B分别是某微粒的结构示意图,回答下列问题。
(1)若A微粒表示带2个单位正电荷的阳离子,则该离子的离子符号为();
(2)若B微粒表示某元素的原子,则y=(),该原子在化学反应中容易()(填“失去”或“得到”)电子。
A.石块的质量是 46.8g
B.石块的体积是 18cm3
C.石块的密度是 2.6×103kg/m3
D.若先测石块的体积,最终测得石块的密度会偏小
合成与制备:
(1)用化学反应方程式表示从海水提取溴的过程。
(2)用化学方法制备单质F,的步骤是
①在HF,KF存在下,用KMnO4氧化H2O2,制备K2MnF6;
②SbCl5和HF反应制备SbF5;
③K2MnF6和SbF5反应制得MnF4;
④不稳定的MnF4分解成MnF3和F2。
试写出以上各步的反应方程式。
(3)工业生产中以KCl为原料制备KClO和KClO3,试用化学反应方程式表示。
(4)以KBr为主要原料制备KBrO4,试用化学反应方程式表示。
(5)试说明实验室中制备SnCl4和AH3的方法,并写出化学反应方程式。
(6)试说明以TiO2和Cl2为主要原料制备TiCl4的具体方法,并写出化学反应方程式。
(7)工业上电解冷的NaCl稀溶液生产NaClO3试说明其过程并写出化学反应方程式。
到白色固体(C)。向(C)的溶液中加入AgNO3溶液生成白色沉淀(D)。向(A)的水溶液中加入CaCl2溶液有白色沉淀(E)生成,(E)溶于盐酸,不溶于NaOH溶液。试给出(A),(B),(C),(D)和(E)所代表的物质的化学式,并用化学反应方程式表示各过程。
合成与制备:
(1)FeCl3催化氯化二硫化碳制备四氯化碳;
(2)用化学反应方程式表示以SiO2为原料生产粗硅,再经提纯得到纯硅的过程;
(3)用化学反应方程式表示以二氧化硅为原料制备甲硅烷及制备纯的甲硅烷的过程;
(4)以硼砂为原料制取B2O3;
(5)以方铅矿(PbS)为原料制备二氧化铅;
(6)如何以二氧化硅为原料制备水玻璃?
(7)如何以水玻璃为原料制备变色硅胶?
(8)如何配制SnCl2溶液?
A.分子运动速率加快,使反应物分子的碰撞机会增多
B.反应物分子的能量增加,活化分子百分数增大,有效碰撞次数增多
C.该化学反应的过程是吸热的
D.该化学反应的过程是放热的
①活化分子间的碰撞不一定能发生化学反应
②普通分子间的碰撞有时也能发生化学反应
③增大反应物浓度,可增大单位体积内活化分子数,从而使有效碰撞次数增多
④有气体参加的化学反应,若增大压强(即缩小反应容器的体积),可增大活化分子的百数,从而使反应速率增大
⑤化学反应的实质是旧化学键断裂和新化学键形成的过程
⑥催化剂能增大活化分子百分数,从而增大化学反应速率
A.1个
B.2个
C.3个
D.4个
A、向国家安全机关寻求庇护
B、不能怂,跟李某拼了
C、反水,和安全机关说自己搞错了