 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
以下各组中的离子,()能在溶液中大量共存。
A.Cu2+、Ba2+、C1-、SO42-
B.K+、Na+、OH-、C1-
C.Na+、H+、SO42-、OH-
D.H+、Na+、Cl-、CO32-
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
A.Cu2+、Ba2+、C1-、SO42-
B.K+、Na+、OH-、C1-
C.Na+、H+、SO42-、OH-
D.H+、Na+、Cl-、CO32-
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“以下各组中的离子,()能在溶液中大量共存。”相关的问题
更多“以下各组中的离子,()能在溶液中大量共存。”相关的问题
A.S2-、Na+、ClO-、OH-
B.Na+、HCO3-、Cl-、H+
C.Na+、Al3+、Cl-、SO42-
D.H+、Fe2+、NO3-、SO42-
A.K+,HCO3-,Cl-,SO42-
B.S2-,CO32-,Cl-,K+
C.K+,Cu2+,SO42-,Na+
D.K+,Cs+,NO3-,SO42-
室温下,在强酸性溶液中能大量共存的离子组是()。
A.Na+、Ca2+、ClO-、Br-
B.K+、Na+、CO32-、HCO3-
C.NH4+、Fe3+、Cl-、NO3-
D.Ba2+、Cu2+、Cl-、SO42-
A.甲、乙两溶液的pH不可能相同
B.甲、乙两种溶液中加入Al粉都一定会产生H2
C.HCO3-不可能在甲、乙两溶液中大量共存
D.甲不可能是盐溶液,乙不可能是酸或碱溶液
A.减少玻璃电极的不对称电势
B.玻璃PH电极能测量带氟离子的液体
C.玻璃PH电极只能在一定的温度范围内正常工作
D.玻璃电极在PH值为1~14溶液中能准确测量
A.溶液中Pb2+和I-浓度都增大
B.溶度积常数增大
C.沉淀溶解平衡向左移动
D.离子积IP增大
E.对平衡无影响
某同学在家中进展化学试验,根据图1连接好线路发觉灯泡不亮,根据图2连接好线路发觉灯泡亮,由此得出的结论正确的选项是()。
A.NaCl是非电解质
B.NaCl溶液是电解质
C.NaCl在水中电离出可以自由移动的离子
D.NaCl溶液中水电离出大量的离子
生产上用过量烧碱溶液处理某矿物(含Al2O3、MgO),过滤后得到的滤液用NaHCO3溶液处理,测得溶液pH、n[Al(OH)3]随加入NaHCO3溶液体积变化的曲线如下图所示。下列有关说法不正确的是()。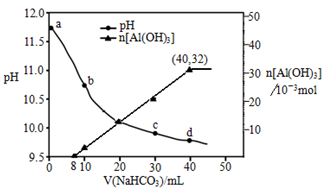
A.生成沉淀的离子方程式为HCO3-+AlO2-+H2O=Al(OH)3↓+CO32-
B.b点与c点溶液所含微粒种类相同
C.a点溶液中大量存在的离子是Na+、AlO2-、OH-
D.NaHCO3溶液的物质的量浓度为0.8mol/L
3.基体金属:形成合金(产物中金属活度小于纯金属,使平衡电位正移,有利于还原反应)
4.欠电势沉积(当金属原子在异种金属电极还原时,有时可以观察到:当电极电势显著正于沉积金属的标准电势时,金属离子就能在基底上还原,生成单原子层厚度的沉积层)