题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
[主观题]
若在用隔板隔开的两密闭容器中分别装有同温同压但体积不同的氢气,若抽掉隔板,让两部分的气体
充分混合,因为氢气活动空间增大,混乱度增加,所以混合过程的熵变大于零。该说法是否正确,并说明理由?
查看答案
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“若在用隔板隔开的两密闭容器中分别装有同温同压但体积不同的氢气…”相关的问题
更多“若在用隔板隔开的两密闭容器中分别装有同温同压但体积不同的氢气…”相关的问题
(1)保持容器内温度恒定抽去隔板,计算气体混合后的压力;
(2)分别计算混合气体中H2和 N2的分压;
(3)分别计算混合气体中H2和N2的分体积.
如图所示,带隔板的容器内,两侧分别有同温同乐的氢气与氮气,二者均可视为理想气体。
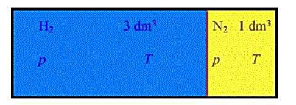
(1)保持容器内温度恒定时抽去隔板,且隔板本身的体积可忽略不计,试求两种气体混合后的压力。
(2)隔板抽取前后,H2及N2的摩尔体积是否相同?
(3)隔板抽取后,混合气体中H2及N2的分压立之比以及它们的分体积各为若干?
刚性绝热容器中间用隔板分为两部分,A 中存有高压空气,B 中保持真空。若将隔板抽去,容器中空气的热力学能将____。能若隔板上有一小孔,气体泄漏入B 中,分析A、B 两部分压力相同时,A部分气体的热力学能将_______,B分气体的热力学能将______。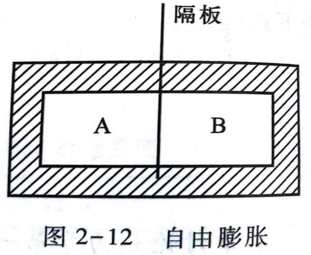
A、不变 变大 变小
B、不变;变小;变大
C、不变 不变 不变
D、变大 变小 不变
A.保持不变
B.增加
C.降低
D.无法判断
(s).现将隔板撤掉,整个系统达到热平衡,求末态温度t及过程的△H.已知:Ar(g)和Cu(s)的摩尔定压热容Cp,m分别为20.786J·mol-1·K-1及24.435J·mol-1·K-1,且假设均不随温度而变化.
现将隔板撤掉,整个系统达到热平衡,求末态温度t及过程的ΔH.已知:Ar(g)和Cu(s)的摩尔定压热容Cp·m分别为20.786J·mol-1·K-1及24.435J·mol-1·K-1,且假设均不随温度而变。