 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
下列说法正确的是()
A.24 g镁与27 g铝中,含有相同的质子数
B.同等质量的氧气和臭氧中,电子数相同
C.1 mol重水与1 mol水中,中子数比为2∶1
D.1 mol乙烷和1 mol乙烯中,化学键数相同
 答案
答案
B、同等质量的氧气和臭氧中,电子数相同
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
A.24 g镁与27 g铝中,含有相同的质子数
B.同等质量的氧气和臭氧中,电子数相同
C.1 mol重水与1 mol水中,中子数比为2∶1
D.1 mol乙烷和1 mol乙烯中,化学键数相同
 答案
答案
B、同等质量的氧气和臭氧中,电子数相同
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“下列说法正确的是()”相关的问题
更多“下列说法正确的是()”相关的问题
A.Na+:钠元素的化合价为+1价
B.Mg(正上方标+2):1个镁离子带2个单位的正电荷
C.2NO2:2个二氧化氮分子
D.2H:1个氢分子由2个氢原子构成
A.Na2O2遇到湿润的紫色石蕊试纸后,石蕊试纸最终变成蓝色
B.Na2O2与CO2反应生成0.1 mol O2时转移电子0.2 mol
C.Na2O2用于呼吸面具,活性炭用于防毒面具,两者原理相同
D.向饱和烧碱溶液中加入2 g Na2O2,充分反应完后,溶液中c(Na+)不变
A.正极发生的电极反应为H2O2+2H++2e- = 2H2O
B.电池总反应为Mg+H2O2 = Mg(OH)2
C.工作时,正极周围海水的酸性增强
D.电池工作时,溶液中的H+向负极移动
A.M、N全部变成了P
B.反应已经停止
C.反应混合物中各组分的浓度不再改变
D.v(M)∶v(N)=2∶1
A.固体混合物中镁元素的质量为4.8g
B.反应后所得溶液中溶质的质量为24g
C.固体混合物中镁元素质量为2.4g
D.反应后所得溶液中溶质的质量为12g
我国是世界产镁大国,金属镁的产量居世界前列。一种由白云石(主要成分为CaO▪MgO,含少量SiO2、A12O3、Fe2O3等杂质)冶炼金属镁的工艺流程如图: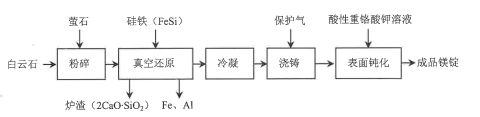 已知:萤石的主要成分是CaF2,用于降低真空还原反应的活化能。
已知:萤石的主要成分是CaF2,用于降低真空还原反应的活化能。
回答下列问题:
(1)①粉碎的主要目的()。
②萤石在真空还原反应中的作用是()(填标号)。
A.氧化剂B.还原剂C.催化剂
(2)Mg2+、Ca2+、Fe3+、Fe2+、A13+五种离子的氧化性由强到弱的顺序为Fe3+>Fe2+>()(用离子符号表示)。
(3)结合流程以及如图温度对MgO还原率的影响关系,真空还原反应温度的最佳选择为();高温真空还原时,CaO、MgO和FeSi反应生成单质镁的化学方程式为()。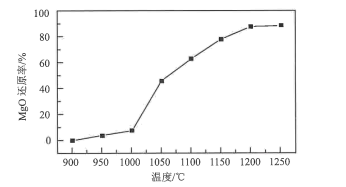 (4)液态镁浇铸成镁锭时,通入的保护气不可选用N2或CO2,其原因是()。
(4)液态镁浇铸成镁锭时,通入的保护气不可选用N2或CO2,其原因是()。
(5)镁锭冷却后,用酸性K2Cr2O7溶液进行表面钝化形成致密的氧化物保护膜,还原产物为Cr3+。该反应的离子方程式为()。
(6)为测定镁锭的纯度,称取a()g除去氧化膜的成品镁锭样品溶于足量稀硫酸中,配成250mL溶液。取25mL该溶液,用0.1000mol/L的EDTA标准溶液进行滴定(杂质不干扰滴定),三次滴定平均消耗EDTA标准溶液V()mL(己知Mg2+与EDTA反应的化学计量数之比为1:1)。该样品的纯度为()%。
A.在上是减函数
B.其图象关于直线x=对称
C.函数g(x)是偶函数
D.在区间上的值域为[-,2]
A.24%
B.20%
C.20.8%
D.25%
瓶中,分别加入5%锶盐溶液2ml后,用蒸馏水稀释至刻度。然后与蒸馏水交替喷雾测定其吸光度。其数据如下所示,计算自来水中镁的量(mg/L)。

A.v(X)= 0.10 mol / (L•min)
B.Y的转化率为25%
C.反应物总能量大于生成物总能量
D.平衡时,c(X):c(Y):c(Z)=1:3:2