 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
[主观题]
当SrCO3固体在pH=8.60的缓冲溶液中达到平衡后,溶液中[Sr2+]=2.2×10-4mol·dm-3,试计算SrCO3的溶度积常数.
查看答案
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“当SrCO3固体在pH=8.60的缓冲溶液中达到平衡后,溶液…”相关的问题
更多“当SrCO3固体在pH=8.60的缓冲溶液中达到平衡后,溶液…”相关的问题
由一元弱酸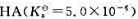 和它的共轭碱NaA组成的缓冲溶液中,HA的浓度为0.25mol·L-1.若在100mL此缓冲溶液中加入5.0mmolNaOH固体,溶液的pH变为5.60。计算加入NaOH固体前缓冲溶液的pH.
和它的共轭碱NaA组成的缓冲溶液中,HA的浓度为0.25mol·L-1.若在100mL此缓冲溶液中加入5.0mmolNaOH固体,溶液的pH变为5.60。计算加入NaOH固体前缓冲溶液的pH.
电池:(一)玻璃电极|缓冲溶液(pH=4.03)||饱和甘汞电极(),测得电动势为0.270V,当已知pH的缓冲溶液换成某一未知液时,测得电动势为0.304V,求未知液的pH。
答:
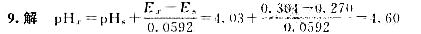
欲配制pH=5.0的缓冲溶液,应在20mL.0.1mol·L-1HAc溶液中加入固体NaAc多少克?(忽略溶液体积的变化) 。已知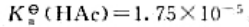
A.小肠液的pH有利于药物的吸收
B.小肠液的pH有利于药物的稳定
C.药物在小肠液中离子型比例增大
D.小肠粘膜具有巨大的表面积
E.药物在小肠液中的溶解度大,溶出速度加快