 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
[主观题]
已知化学反应在1000K时平衡常数为Kp=1.36,试问当各成分的原始浓度分别为[CO]=5kmol/m
已知化学反应![已知化学反应在1000K时平衡常数为Kp=1.36,试问当各成分的原始浓度分别为[CO]=5kmol](https://img2.soutiyun.com/ask/2020-12-03/975839097087176.png) 在1000K时平衡常数为Kp=1.36,试问当各成分的原始浓度分别
在1000K时平衡常数为Kp=1.36,试问当各成分的原始浓度分别
为[CO]=5kmol/m3,[H2O]=3kmo/m3,[CO2]=3kmol/m³及[H2]=3kmol/m3时反应向何方向进行?
查看答案
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
已知化学反应![已知化学反应在1000K时平衡常数为Kp=1.36,试问当各成分的原始浓度分别为[CO]=5kmol](https://img2.soutiyun.com/ask/2020-12-03/975839097087176.png) 在1000K时平衡常数为Kp=1.36,试问当各成分的原始浓度分别
在1000K时平衡常数为Kp=1.36,试问当各成分的原始浓度分别
为[CO]=5kmol/m3,[H2O]=3kmo/m3,[CO2]=3kmol/m³及[H2]=3kmol/m3时反应向何方向进行?
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“已知化学反应在1000K时平衡常数为Kp=1.36,试问当各…”相关的问题
更多“已知化学反应在1000K时平衡常数为Kp=1.36,试问当各…”相关的问题
已知反应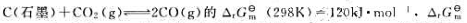 (1000K)=-3.4kJ·mol-1,计算(1) 在标准状态及温度分别为298K和1000K时的标准平衡常数;(2)当1000K时,p(CO)=200kPa,p(CO2)=800kPa,判断该反应方向。
(1000K)=-3.4kJ·mol-1,计算(1) 在标准状态及温度分别为298K和1000K时的标准平衡常数;(2)当1000K时,p(CO)=200kPa,p(CO2)=800kPa,判断该反应方向。
A.Kp① >Kp②
B.Kp①
C.Kp①=Kp②
D.无法确定
已知300时,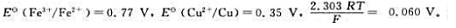 则可逆反应:
则可逆反应: 在300K时的标准平衡常数为()
在300K时的标准平衡常数为()
A、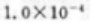
B、
C、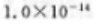
D、
A.50
B.0.01
C.10
D.无法确定
已知生产水煤气反应:
C(s)+H2O(g)=CO(g)+H2(g)
在1000K时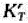 =1.00,若于密闭反应罐中通入1×105Pa的水汽与足量的红热碳反应,试确定平衡时诸气体的压力和水汽的转化率.
=1.00,若于密闭反应罐中通入1×105Pa的水汽与足量的红热碳反应,试确定平衡时诸气体的压力和水汽的转化率.
已知反应:

在45℃时,将0.0030mol的N2O.注入容积为0.50L的真空容器中,系统达平衡时,压力为26.3kPa,试计算:
(1)45℃时N2O4,的分解率及反应的标准平衡常数:
(2)25℃时反应的标准平衡常数;
(3)25℃时反应的标准摩尔熵变;
(4)反应的标准摩尔Cibbs函数变随温度变化的函数关系式.
已知A(g)的分解反应为一级反应。在560K的真空密闭恒容容器中充入初始压力为21.33kPa的氮甲烷气体,反应进行1000s时测得系统的总压为22.73kPa,求速率常数kp,A及半衰期t1/2。