 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
[判断题]
用0.1mol/LNaOH分别滴定同浓度的弱酸A(pKa=4.0)与弱酸B(pKa=3.0)滴定的pH突跃范围是弱酸A比弱酸B大。()
查看答案
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“用0.1mol/LNaOH分别滴定同浓度的弱酸A(pKa=4…”相关的问题
更多“用0.1mol/LNaOH分别滴定同浓度的弱酸A(pKa=4…”相关的问题
枸橼酸的离解常数分别为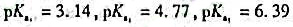 ,如用0.1mol/LNaOH滴定同浓度的枸橼酸溶液,滴定曲线上有()个突跃。
,如用0.1mol/LNaOH滴定同浓度的枸橼酸溶液,滴定曲线上有()个突跃。
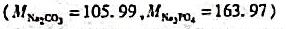
A.9.7~4.3
B.8.7~4.3
C.8.7~5.3
D.10.7~3.3
准确量取30.00ml弱酸HA,加水稀释至100ml,在下列电池中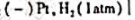
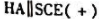 为测定电池,以0.1000mol/LNaOH溶液滴定弱酸HA溶液。当酸被中和一半时,电池电动势为0.524V;化学计量点时,电池电动势为0.749V。(1)计算弱酸HA的Ka;(2)原弱酸HA的浓度是多少?(φSCE=0.242V)。
为测定电池,以0.1000mol/LNaOH溶液滴定弱酸HA溶液。当酸被中和一半时,电池电动势为0.524V;化学计量点时,电池电动势为0.749V。(1)计算弱酸HA的Ka;(2)原弱酸HA的浓度是多少?(φSCE=0.242V)。
A.氨水(Kb=1.8×10-5)
B.苯酚(Kb=1.1×10-10)
C.NH4+
D.H3BO3(Ka=5.8×10-10)
A.0.1mol/LNH4Cl+0.2mol/LNaOH
B.0.1mol/LNH3+0.2mol/LNH4Cl
C.0.2mol/LNH3+0.1mol/LHCl
D.0.2mol/LNH4Cl+0.1mol/LNaOH
A.#图片0$#
B.#图片1$#
C.#图片2$#
D.#图片3$#
A.H2SO4溶液和HAc溶液中的氢离子浓度相等
B.H2SO4溶液的氢离子浓度是HAc溶液的氢离子浓度的2倍
C.H2SO4溶液的浓度与HAc溶液的浓度相等
D.H2SO4溶液的浓度是HAc溶液的浓度的1/2
A.99.1%
B.100.2%
C.98.2%
D.97.5%
E.96.5%