 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
[主观题]
用0.1000mol/LHCl溶液滴定0.1000mol/LNa2CO3溶液至pH5.00。计算有百分之几的Na2CO≇
用0.1000mol/LHCl溶液滴定0.1000mol/LNa2CO3溶液至pH5.00。计算有百分之几的Na2CO3变成了H2CO3?剩下的主要组分是什么?如果煮沸溶液以除尽CO2,冷却后溶液的pH为多少?(H2CO3的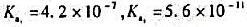 )
)
查看答案
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
用0.1000mol/LHCl溶液滴定0.1000mol/LNa2CO3溶液至pH5.00。计算有百分之几的Na2CO3变成了H2CO3?剩下的主要组分是什么?如果煮沸溶液以除尽CO2,冷却后溶液的pH为多少?(H2CO3的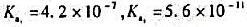 )
)
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“用0.1000mol/LHCl溶液滴定0.1000mol/L…”相关的问题
更多“用0.1000mol/LHCl溶液滴定0.1000mol/L…”相关的问题
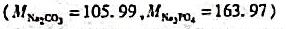
A.0.86~1.26V
B.0.86~1.44V
C.0.68~1.26V
D.0.68~1.44V
A.8.74~10.70
B.6.74~9.70
C.6.74~10.70
D.5.74~9.70
在酸性条件下,用0.1000mol/L的K2Cr2O7溶液滴定0.1000m0/L20.00mFe2+,已知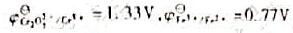 ,合适的指示剂为()。
,合适的指示剂为()。
A.亚甲蓝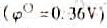
B.邻二氮菲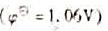
C.二苯胺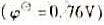
D.变胺蓝
A、NaOH
B、NaHCO3
C、Na2CO3
D、NaOH+Na2CO3
A.0.2000mol·L-1
B.0.1000mol·L-1
C.0.05000mol·L-1
D.0.02500mol·L-1