 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
金属M溶于稀盐酸时生成MCl2,其磁矩为5.0B.M.。在无氧操作条件下,MCl2溶液遇NaOH溶液生成白色沉淀A。A接触空气
金属M溶于稀盐酸时生成MCl2,其磁矩为5.0B.M.。在无氧操作条件下,MCl2溶液遇NaOH溶液生成白色沉淀A。A接触空气逐渐变绿或蓝绿,最后变成棕色沉淀B。灼烧时,B转化为棕红色粉末C。B不溶于NaOH溶液,B与草酸氢钾溶液在加热条件下得黄色溶液,蒸发、浓缩后有绿色晶体D析出。
B溶于盐酸生成黄色溶液E。E与KI溶液作用有I2生成,再加过量的NaF,I2又消失。若向B的浓Na0H悬浮液中通入Cl2气时可得到紫红色溶液F。向F中加入BaCl2时有红棕色沉淀G生成。G为强氧化剂。请给出A,B,C,D,E,F,G所代表的化合物.并写出反应方程式。
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案


 更多“金属M溶于稀盐酸时生成MCl2,其磁矩为5.0B.M.。在无…”相关的问题
更多“金属M溶于稀盐酸时生成MCl2,其磁矩为5.0B.M.。在无…”相关的问题
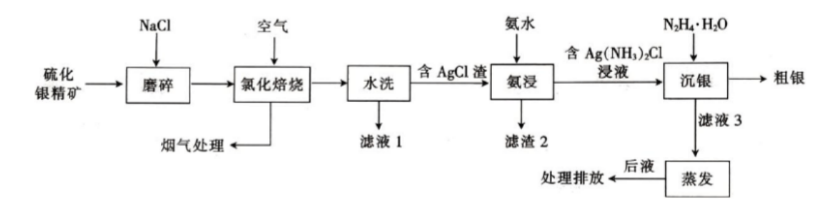 已知:氯化焙烧时,氧化物不参与反应,硫化物转化为氯化物;氯化铅不溶于水,溶于氯化钠溶液。
已知:氯化焙烧时,氧化物不参与反应,硫化物转化为氯化物;氯化铅不溶于水,溶于氯化钠溶液。
















