 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
向Al2(SO4)a和CuSO4的混合溶液中放入一个铁钉,其变化是()
A.生成Al、H2和Fe2+
B.生成Al、Cu和Fe2+
C.生成Cu和Fe2+
D.生成Cu和Fe3+
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
A.生成Al、H2和Fe2+
B.生成Al、Cu和Fe2+
C.生成Cu和Fe2+
D.生成Cu和Fe3+
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“向Al2(SO4)a和CuSO4的混合溶液中放入一个铁钉,其…”相关的问题
更多“向Al2(SO4)a和CuSO4的混合溶液中放入一个铁钉,其…”相关的问题
A.用Na2S溶液和Al2(SO4)3溶液反应制取Al2S3固体
B.用加热蒸发K2CO3溶液的方法获得K2CO3晶体
C.用Na2S溶液和CuSO4溶液反应制取CuS固体
D.加热MgSO4溶液制取MgSO4固体
A.混合物X中必定含有Na2CO3,不含Al2(SO4)3
B.溶液Z中溶质主要是钠盐,且必含NaHCO3
C.灼烧沉淀Y,可以得到黑色物质
D.往溶液Z中加入Cu粉,若不溶解,说明X中不含FeCl3
某地有软锰矿和闪锌矿两座矿山,它们的组成如下:软锰矿:MnO2含量≥65%,SiO2含量约20%,Al2O3含量约4%,其余为水分;闪锌矿:ZnS含量≥80%,FeS、CuS、SiO2含量约7%,其余为水分。科研人员开发了综合利用这两种资源的同槽酸浸工艺,工艺流程如以下图所示。
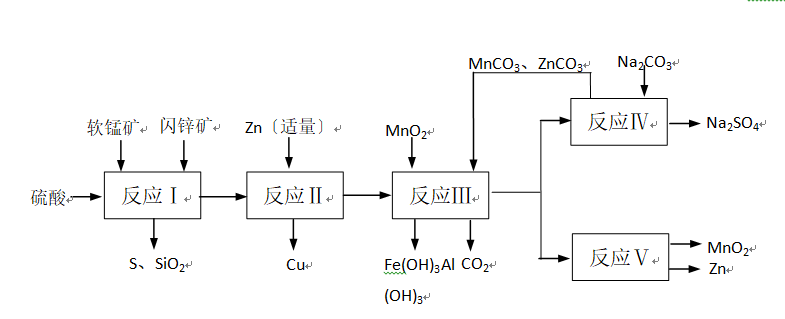
请答复以下问题:
问题一、反应Ⅰ后过滤所得滤液中含有MnSO4、ZnSO4、CuSO4、Fe2(SO4)3、Al2(SO4)3等。试写出反应Ⅰ中生成CuSO4的化学方程式()。
问题二、反应Ⅱ加入适量锌的作用是()。如果锌过量,还会进一步发生反应的离子方程式为()。
问题三、反应Ⅴ的条件是电解,电解时均用惰性电极,阳极发生的电极反应可表示为()。
问题四、本工艺所用的原料除软锰矿、闪锌矿、硫酸外还需要()等原料。
A.①
B.②
C.③
D.④
 分别为1.36V,1.07V,0.54V。今有一种Cl-,Br-,I-的混合溶液,标准状态时能氧化I-而不氧化Br-和Cl-的物质是( )
分别为1.36V,1.07V,0.54V。今有一种Cl-,Br-,I-的混合溶液,标准状态时能氧化I-而不氧化Br-和Cl-的物质是( )A.KMnO4(
B.MnO2(
C.Fe2(SO4)3(
D.CuSO4(
A.将铜丝插入稀硝酸中:Cu+4H++2NO =Cu2++2NO2↑+H2O
B.向Fe2(SO4)3溶液中加入过量铁粉:Fe3++Fe=2Fe2+
C.向Al2(SO4)3溶液中加入过量氨水:Al3++3NH3·H2O=Al(OH)3↓+3NH
D.向Na2SiO3溶液中滴加稀盐酸:Na2SiO3+2H+=H2SiO3↓+2Na+
A.将铜丝插入稀硝酸中:Cu + 4H+ + 2NO3- === Cu2+ + 2NO2↑ + H2O
B.向Fe2(SO4)3溶液中加入过量铁粉:Fe3+ + Fe === 2Fe2+
C.向Al2(SO4)3溶液中加入过量氨水:Al3+ + 3NH3·H2O === Al(OH)3↓ + 3NH4+
D.向Na2SiO3溶液中滴加稀盐酸:Na2SiO3 + 3H+ === H2SiO3↓ + 3Na+
浓度为m的Al2(SO4)3溶液中正、负离子的活度系数分别为γ+和γ-,则γ±=_______,平均活度a±=_______。
A.NaOH溶液和AlCl3溶液
B.稀H2SO4与Al(OH)3
C.Al和NaOH溶液
D.氨水与Al2(SO4)3溶液