 更多“含硫化钠的废水用酸性溶液回收。()”相关的问题
更多“含硫化钠的废水用酸性溶液回收。()”相关的问题
A.所用显色剂有硫代乙酰胺、硫化钠以及硫化铅
B.标准铅溶液至少提前一天配置,且配置与贮藏用的玻璃容器均不得含铅
C.烧灼后硫代乙酰胺法适用于难溶于水或不溶于水、稀酸或乙醇的药品等
D.显色剂硫化钠对玻璃有腐蚀性,因此需临用前新制
E.对于有色溶液无法处理的,可用第三法硫化钠法进行检查
A.用含5%P204及4.5%LMS-2的煤油为膜相,6mol/L盐酸为膜内相,油内比为3:1,可从3%硫酸铵稀土浸出液中逐一分离出所有单个的纯稀土化合物;
B.用含P2042~4%,T1542%的煤油为膜相,以3mol/l硫酸为内相从粘胶工业含锌废水中分离锌,可将锌富集到14g/l而返回粘胶工业使用;
C.提铜方面,可以用含Lix64的乳状液膜回收铜,回收率达到95%;
D.用充注P507的螺旋型支撑液膜进行了分离镍钴的实验研究,结果表明,溶液通过一次其中99.7%的钴即被提取,且反萃液中钴浓度可高于料液中70000倍
随着工业的迅速发展,产生的废水对水体的污染也日趋严重。通过控制溶液的pH对工业废水中的金属离子进行别离是实际工作中经常使用的方法。下表是常温下金属氢氧化物的Ksp(沉淀溶解平衡常数)和金属离子在某浓度下开始沉淀所需的pH(表中浓度为相应pH时溶液中有关金属离子产生沉淀的最小浓度;当溶液中金属离子浓度小于10-5mol•L-1时通常认为该离子沉淀完全)。 问题一、某厂排出的废水中含有Cu2+和Fe3+,测得其浓度均小于0.1mol•L-l。为除去其中的Fe3+,回收铜,需控制的pH范围是()。
问题一、某厂排出的废水中含有Cu2+和Fe3+,测得其浓度均小于0.1mol•L-l。为除去其中的Fe3+,回收铜,需控制的pH范围是()。
问题二、为了处理含有Cr2O72-酸性溶液的工业废水,采用如下方法:向废水中加人适量NaCl,以Fe为电极进行电解,经过一段时间,有Cr(OH)3和Fe(OH)3沉淀生成排出,从而使废水中铬含量低于排放标准
①Cr2O72-转变为Cr3+的离子方程式为()。
②pH对废水中Cr2072-去除率的影响如右图。你认为电解过程中溶液的pH取值在()范围内对降低废水中的铬含量最有利,请说明理由:()。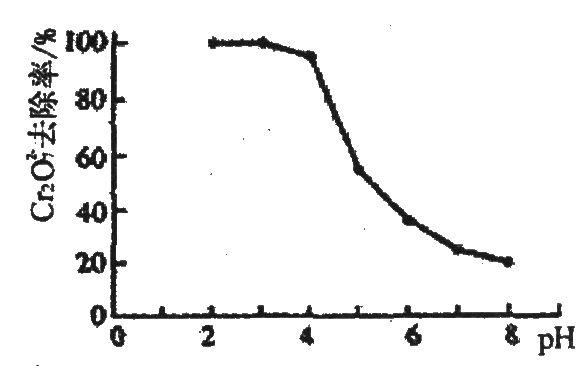
问题三、沉淀转化在生产中也有重要应用。例如,用Na2C03溶液可以将锅炉水垢中的CaS04转化为较疏松而易清除的CaC03,该沉淀转化到达平衡时,其平衡常数K=()。(已知Ksp(CaS04)=9.1x10-6,Ksp(CaC03)=2.8x10-9)
A.金刚石和石墨在氧气中燃烧生成同一种产物,说明金刚石和石墨的组成元素相同
B.铁丝可以在氧气中燃烧,说明氧气具有可燃性
C.用pH试纸检验某工厂排出的废水,结果pH=3,说明废水呈较强的酸性
D.将酚酞分别滴入烧碱溶液和石灰水中,溶液均变红,说明碱溶液能使酚酞试液变红


 如果结果不匹配,请
如果结果不匹配,请 

















