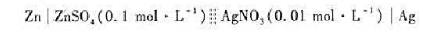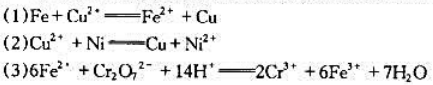更多“某原电池反应达到平衡时,电动势等于零,则正、负两极的标准电极…”相关的问题
更多“某原电池反应达到平衡时,电动势等于零,则正、负两极的标准电极…”相关的问题
第1题
将铜片插入盛有1.0dm32.0mol·dm-3Cu2+溶液的烧杯中,将锌片插入盛有1.0dm3,2
.0mol·dm-3Zn2+溶液的烧杯中,组成原电池。
点击查看答案
(1)写出原电池符号、电池反应式;
(2)查标准电极电势表,求该原电池的标准电动势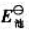 ;
;
(3)当电池反应进行到c(Cu2+)=1.0mol·dm-3时,试计算原电池的电动势E池。
第2题
已知反应2Cr3++3Cl2+7H2O=Cr2O72-+6C1-+14H+(Cr2⌘
已知反应2Cr3++3Cl2+7H2O=Cr2O72-+6C1-+14H+(Cr2⌘
点击查看答案
已知反应
2Cr3++3Cl2+7H2O=Cr2O72-+6C1-+14H+
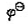 (Cr2O72-/Cr3+)=1.33V,
(Cr2O72-/Cr3+)=1.33V,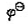 (Cl2/CI-)=1.36V,F=95500J·V-1·mol-2若在298K时组成原电池。
(Cl2/CI-)=1.36V,F=95500J·V-1·mol-2若在298K时组成原电池。
(1)写出该原电监的电池符号,并计算标准电动势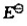 ;(2)计算
;(2)计算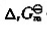 (298K)并判断反应进行的方向;(3)计算标准平衡常数
(298K)并判断反应进行的方向;(3)计算标准平衡常数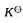 ;(4)若c(H+)=10mol·dm-3,其他离子浓度均为标准浓度,求原电池的电动势E并判断反应进行的方向
;(4)若c(H+)=10mol·dm-3,其他离子浓度均为标准浓度,求原电池的电动势E并判断反应进行的方向
第5题
在950℃时,可逆反应的标准平衡常数则在此温度下上述反应达到平衡时O2的分压为()。A、1.4kPa
在950℃时,可逆反应的标准平衡常数则在此温度下上述反应达到平衡时O2的分压为()。A、1.4kPa
点击查看答案
在950℃时,可逆反应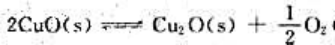 的标准平衡常数
的标准平衡常数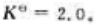 则在此温度下上述反应达到平衡时O2的分压为()。
则在此温度下上述反应达到平衡时O2的分压为()。
A、1.4kPa
B、4.0kPa
C、140kPa
D、400kPa
第6题
若原电池的两金属电极极均处于零电荷电位下,则该原电池的电动势等于这两块金属的接触电位差。()
若原电池的两金属电极极均处于零电荷电位下,则该原电池的电动势等于这两块金属的接触电位差。()
点击查看答案
此题为判断题(对,错)。
第7题
合成氨反应N2+3H2=2NH3在某温度下建立平衡,达到平衡时,各组分浓度为[N2]=30mo
l·dm-3,[H2]=2.0mol·dm-3,[NH3]=4.0mol·dm-3,求该反应的平衡常数Kc.N2及H2的起始浓度及各自转化率是多少?(设起始时体系中只有氢气和氨气)
点击查看答案
第8题
有如下原电池,其两极均为金属-金属离子电极:当c(A2+)=c(B2+)时,电动势为0.78V。放
有如下原电池,其两极均为金属-金属离子电极:当c(A2+)=c(B2+)时,电动势为0.78V。放
点击查看答案
有如下原电池,其两极均为金属-金属离子电极:

当c(A2+)=c(B2+)时,电动势为0.78V。放电一段时间后电动势值减半,求此时的c(A2+)/c(B2+)。
第9题
已知反应当达到平衡后,若压缩反应容器;若升高温度,Z的物质的量的体积,Z的物质的量();若升高温
已知反应当达到平衡后,若压缩反应容器;若升高温度,Z的物质的量的体积,Z的物质的量();若升高温
点击查看答案
已知反应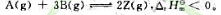 当达到平衡后,若压缩反应容器;若升高温度,Z的物质的量的体积,Z的物质的量();若升高温度,Z的物质的量();加入A,则Z的物质的量()。
当达到平衡后,若压缩反应容器;若升高温度,Z的物质的量的体积,Z的物质的量();若升高温度,Z的物质的量();加入A,则Z的物质的量()。
第11题
某反应(能完全反应)活化能的实验测定在两个不同温度T1,T2,下进行.两次实验均从相同的
某反应(能完全反应)活化能的实验测定在两个不同温度T1,T2,下进行.两次实验均从相同的
点击查看答案
初始浓度开始,并都达到相同的转化率,两次实验所笛的时问分别为T1和T2.若反应为一级反应时所求得的活化能为En.1,反应为二级反应时所求得的活化能为En.2o则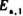 ()
()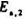 .
.
A.大于
B.等于
C.小于
D.既可能大于,也可能小于


 如果结果不匹配,请
如果结果不匹配,请 
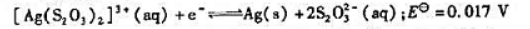
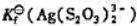 .
.