 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
已知在-5℃,水和冰的密度分别为p(H2O,l)=999.2kg.m-3p(H2O,s)=916.7kg·m-3.在-5℃,水和冰的相平衡压力为59.8MPa.今有-5℃,1kg的水在100kPa下凝固成同样温度下的冰,求过程的ΔG.假设水和冰的密度不随压力变.
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“已知在-5℃,水和冰的密度分别为p(H2O,l)=999.2…”相关的问题
更多“已知在-5℃,水和冰的密度分别为p(H2O,l)=999.2…”相关的问题
设有如下推理规则。
r1:E1→H1LS=100,LN=0.1
r2:E2→H2LS=50,LN=0.5
r3:E3→H3LS=5,LN=0.05
且已知P(H1)=0.02,P(H2)=0.2,P(H3)= 0.4,请计算当证据E1,E2,E3存在或不存
在时P(Hi|Ei)或P(Hi|~Ei)的值各是多少(i=1,2,3)?
设P{X=k}=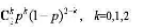
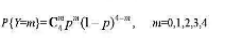 分别为随机变量X,Y的概率分布,如果已知P{X≥1}=5/9,试求P{Y≥1}。
分别为随机变量X,Y的概率分布,如果已知P{X≥1}=5/9,试求P{Y≥1}。
已知298K时下述电池的电动势为1.362V,
(Pt)H2(pθ)|H2SO4(aq)|Au2O3=Au(s)
又知H2O(g)的ΔrGmθ=-228.6kJ·mol-1,该温度下水的饱和蒸汽压为3167Pa,
求在298K时氧气的逸度为多少才能使Au2O3与Au呈平衡?
乙烷裂解生成乙烯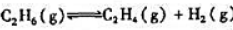 已知在1273K,100.0kPa下,反应达到平衡时,p(C2H6)=2.62kPa,p(C2H4)=48.7kPa,p(H2)=48.7kPa.计算该反应的标准平衡常数Kθ.在实际生产中可在定温定压下采用加入过量水蒸气的方法来提高乙烯的产率(水蒸气作为惰性气体加入),试以平衡移动的原理加以说明.
已知在1273K,100.0kPa下,反应达到平衡时,p(C2H6)=2.62kPa,p(C2H4)=48.7kPa,p(H2)=48.7kPa.计算该反应的标准平衡常数Kθ.在实际生产中可在定温定压下采用加入过量水蒸气的方法来提高乙烯的产率(水蒸气作为惰性气体加入),试以平衡移动的原理加以说明.
已知化学反应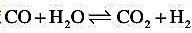 在1000K时平衡常数为Kp=1.36,试问当各成分的原始浓度分别
在1000K时平衡常数为Kp=1.36,试问当各成分的原始浓度分别
为[CO]=5kmol/m3,[H2O]=3kmo/m3,[CO2]=3kmol/m³及[H2]=3kmol/m3时反应向何方向进行?
冰(H2O,s)在100kPa下的熔点为0℃,此条件下的摩尔融化焓 =6.012kJ·mol-1.已知在-10~0℃范围内过冷水(H2O,l)和冰的摩尔定压热容分别为76.28J·mol-1·K-1和37.20J·mol-1·
=6.012kJ·mol-1.已知在-10~0℃范围内过冷水(H2O,l)和冰的摩尔定压热容分别为76.28J·mol-1·K-1和37.20J·mol-1·
K-1.求在常压及-10℃下过冷水结冰的摩尔凝固焓.
已知反应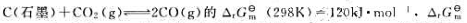 (1000K)=-3.4kJ·mol-1,计算(1) 在标准状态及温度分别为298K和1000K时的标准平衡常数;(2)当1000K时,p(CO)=200kPa,p(CO2)=800kPa,判断该反应方向。
(1000K)=-3.4kJ·mol-1,计算(1) 在标准状态及温度分别为298K和1000K时的标准平衡常数;(2)当1000K时,p(CO)=200kPa,p(CO2)=800kPa,判断该反应方向。
已知C(石墨)和H2的燃烧热分别为-393.5kJ·mol-1及-285.8kJ·mol-1,1mol
甲醛CH3OCH3完全燃烧时,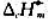 =-1461kJ·mol-1,求:
=-1461kJ·mol-1,求:
(1)甲醚的 ;
(2)已知键焓B.E.(H-H)=436kJ·mol-1,B.E.(C-O)=343kJ·mol-1,B.E.(o-o)=498kJ·mol-1,
B.E.(C-H)=415kJ·mol-1,试用以上数据估算甲醚的 ,比较以上结果,你得到什么结论?