 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
[主观题]
等体积混合O.30mol·L-1的NH3溶液、0.30mol·L-1的NaCN和0.030mol·L-1的Ag
NO3溶液,求平衡时Ag(CN)-2和Ag(NH3)+2法浓度比是多少?已知:
K[Ag(CN)2-]=1.0X1021,K[Ag(NH3)]2+=-1.6X107.
查看答案
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
K[Ag(CN)2-]=1.0X1021,K[Ag(NH3)]2+=-1.6X107.
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“等体积混合O.30mol·L-1的NH3溶液、0.30mol…”相关的问题
更多“等体积混合O.30mol·L-1的NH3溶液、0.30mol…”相关的问题
298K下,0.2mol·L-1的HAc溶液与0.2mol·L-1的NaAc溶液等体积混合后,该溶液的pH为() , 已知:HAc的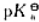 =4.76
=4.76
A.4.75
B.6.25
C.7.00
D.9.25
)2沉淀生成.若此NH3·NH4Cl混合溶液中NH3的浓度0.10mol·L-1,则此混合溶液中NH4Cl的浓度至少为多少?
查附录获取所需酸碱的解离平衡常数,并计算下列溶液的pH。
(1)0.10 mol·dm-3NH3·H2O;
(2)20.0 cm30.100 mol·dm-3HAc溶液加20.0 cm3水稀释;
(3)10.0 dm3纯水中加入1.0 cm31.0×10-3mol·dm-3盐酸;
(4)50cm30.20 mol·dm-3NH3·H2O和50cm30.20 mol·dm-3盐酸的混合溶液;
(5)0.20 mol·dm-3草酸氢钾KHC2O4溶液;
(6)50cm30.40 mol·dm-3NaAc溶液和50cm 0.10 mol·dm-3盐酸的混合溶液;
(7)0.20mol·dm-3H2SO4溶液和 0.40 mol·dm-3Na2SO4溶液等体积混合后所得溶液;
(8)100 cm30.25 mol·dm-3NaH2PO4溶液和50 cm30.35 mol·dm-3Na2HPO4溶液混合后所得溶液。