 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
[主观题]
将带有两通活塞的真空刚性容器置于压力恒定,温度为T0的大气中.现将活寒打开,使大气迅速流人并充满容器,达到容器内外压力相等.求证进入容器斤的气体温度T=γT0.式中γ为大气的热容比.推导时不考虑容器的热容,且大气按一种气体对待.全部进人容器的气体为系统,系统得到流动功.
查看答案
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“将带有两通活塞的真空刚性容器置于压力恒定,温度为T0的大气中…”相关的问题
更多“将带有两通活塞的真空刚性容器置于压力恒定,温度为T0的大气中…”相关的问题
,试求反应
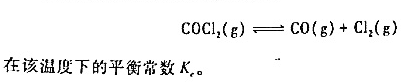
(1)保持容器内温度恒定抽去隔板,计算气体混合后的压力;
(2)分别计算混合气体中H2和 N2的分压;
(3)分别计算混合气体中H2和N2的分体积.
A.两位两通
B.两位三通
C.三位三通
D.三位四通
298K时,苯的饱和蒸气压为12.7kPa,将2.0g苯置于密闭容器内:
(1)若容器的体积为2.0dm3,苯蒸气压力为多少?
(2)若容器的体积为6.0dm3,苯蒸气压力为多少?
A.节气门体上装配了节气门和若干其它必要的装置,如怠速空气控制(IAC)阀、旁通槽、怠速调整螺钉和快怠速阀
B.节气门体上装配了节气门和若干其它必要的装置,如怠速空气控制(IAC)阀、旁通槽、怠速调整螺钉和喷油器
C.燃油压力调节器将进气歧管真空与燃油压力之间的压力差保持在一个恒定水平上
D.燃油压力调节器将燃油喷射压力保持在恒定水平
已知反应:

在45℃时,将0.0030mol的N2O.注入容积为0.50L的真空容器中,系统达平衡时,压力为26.3kPa,试计算:
(1)45℃时N2O4,的分解率及反应的标准平衡常数:
(2)25℃时反应的标准平衡常数;
(3)25℃时反应的标准摩尔熵变;
(4)反应的标准摩尔Cibbs函数变随温度变化的函数关系式.