 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
海水中几种离子的浓度如下:求:(1)c(OH-)浓度多少时,Mg(OH)2开始沉出?已知:K[Mg(OH)≇
海水中几种离子的浓度如下:
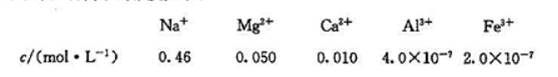
求:(1)c(OH-)浓度多少时,Mg(OH)2开始沉出?已知:K[Mg(OH)2]=5.61X10-12.
(2)在该OH-离子浓度下,是否还有别的离子沉出?已知:K[Al(OH)3]=1.1X10-33,K[Fe(OH)3]=
264X10-39.
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
海水中几种离子的浓度如下:
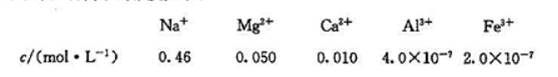
求:(1)c(OH-)浓度多少时,Mg(OH)2开始沉出?已知:K[Mg(OH)2]=5.61X10-12.
(2)在该OH-离子浓度下,是否还有别的离子沉出?已知:K[Al(OH)3]=1.1X10-33,K[Fe(OH)3]=
264X10-39.
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“海水中几种离子的浓度如下:求:(1)c(OH-)浓度多少时,…”相关的问题
更多“海水中几种离子的浓度如下:求:(1)c(OH-)浓度多少时,…”相关的问题
A.次氯酸钠
B.金属离子和氧化物质
C.臭氧
D.氢氧化物
:
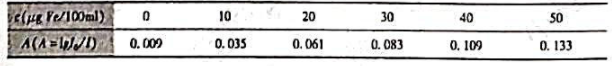
试求:①吸光度-浓度(A-c)的回归方程式;②相关系数;③A=0.050时,试样溶液中亚铁离子的浓度。
将7.00g结晶草酸(H2C2O4·H2O)溶于93.0g水中,所得溶液的密度为1.025g·cm-3。求该溶液的:(1)物质的量浓度;(2)质量摩尔浓度;(3)溶质物质的量分数;(4)质量分数。
已知: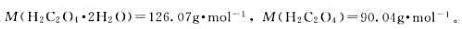
结果。已知
(1) 氧化型浓度增加至10mol·L-1,还原型浓度不变;
(2) 还原型浓度增加至10mol·L-1,氧化型浓度不变;
(3)标准态溶液均稀释10倍。
在105Pa下,20℃时,H2S在水中的溶解度是每体积水溶解2.61体积H2S.
(1)求饱和H2S水溶液中H2S的摩尔浓度.
(2)计算饱和H2S水溶液中的[H+],[HS-]和[S2-].
(3)若调节pH=2.00时,[S2-]为多少?
(4)计算0.1mol·dm-3Na2S中[S2-]和pH值.

已知反应
2Cr3++3Cl2+7H2O=Cr2O72-+6C1-+14H+
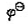 (Cr2O72-/Cr3+)=1.33V,
(Cr2O72-/Cr3+)=1.33V,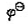 (Cl2/CI-)=1.36V,F=95500J·V-1·mol-2若在298K时组成原电池。
(Cl2/CI-)=1.36V,F=95500J·V-1·mol-2若在298K时组成原电池。
(1)写出该原电监的电池符号,并计算标准电动势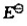 ;(2)计算
;(2)计算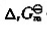 (298K)并判断反应进行的方向;(3)计算标准平衡常数
(298K)并判断反应进行的方向;(3)计算标准平衡常数 ;(4)若c(H+)=10mol·dm-3,其他离子浓度均为标准浓度,求原电池的电动势E并判断反应进行的方向
;(4)若c(H+)=10mol·dm-3,其他离子浓度均为标准浓度,求原电池的电动势E并判断反应进行的方向